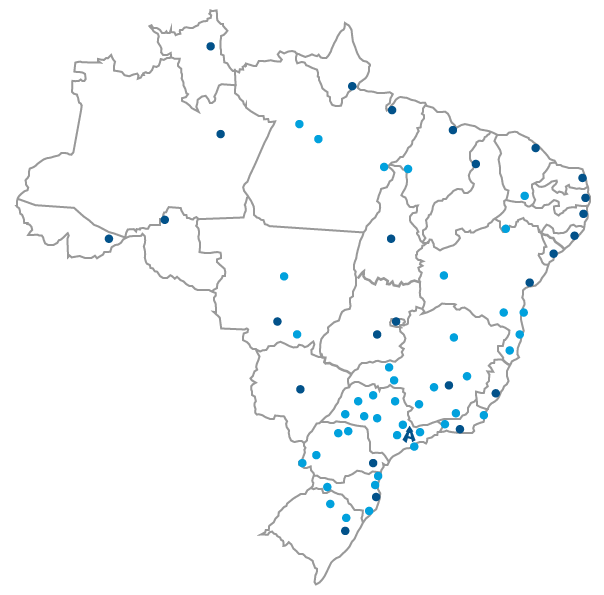
SINÔNIMO DE EXCELÊNCIA NO TRANSPORTE AÉREO E RODOVIÁRIO PARA TODO BRASIL
NOSSOS SEGMENTOS
NOSSOS SERVIÇOS
QUALIDADE É NOSSO FOCO
FROTA E GERENCIAMENTO DE RISCO
FROTA PRÓPRIA IDENTIFICADA E EQUIPE TREINADA!
Nossos veículos e equipe de logística demonstram a qualidade de nossa empresa.
Os veículos são adesivados, possuem baú refrigerado, isotérmico e plataforma hidráulica. Além disso, possuem data loggers que monitoram a temperatura e umidade interna do baú. Os rastreadores são híbridos (comunicação GPRS e Satelital) e nosso gerenciamento de risco é realizado por empresa especializada e homologada pela nossa seguradora.
Nossa equipe é uniformizada e recebe treinamento constante, para atender nossos clientes de forma eficiente. Segundo nosso Manual de Boas Práticas em Transporte, a área é responsável por mais de 70% dos Procedimentos Operacionais Padrões.
Estes são alguns dos aspectos que garantem a segurança dos nossos funcionários, a regularidade e a qualidade dos nossos serviços.
LICENÇAS E AUTORIZAÇÕES
NOSSA HISTÓRIA
ARGHI UMA HISTÓRIA DE SUCESSO!
Fundada em 7 de agosto de 1996, a principal atividade da Arghi é a comercialização dos serviços de transporte aéreo de encomendas e cargas expressas e transporte de carga fracionada e lotação para todo o território nacional, aplicado às instalações da matriz no estado de São Paulo, capital.
Somos reconhecidos no mercado como uma empresa que cumpre com rigor suas obrigações, e ainda colabora para aperfeiçoar os processos de seus clientes.
Qualquer que seja a origem e destino da encomenda, a Arghi é ágil, qualificada e capacitada a realizar o serviço porta-a-porta em todo território nacional.
Por essas e por outras que a Arghi faz melhor, faz muito mais!